Liên Kết Kim Loại Là Liên Kết được Hình Thành Do lực hút tĩnh điện giữa các ion dương kim loại và các electron tự do di chuyển trong mạng tinh thể. Nghe có vẻ phức tạp phải không? Đừng lo, hãy cùng HSE tìm hiểu sâu hơn về loại liên kết thú vị này, từ những khái niệm cơ bản đến ứng dụng thực tiễn trong cuộc sống hàng ngày.
Lực Hút Tĩnh Điện và Biển Electron: Cốt Lõi của Liên Kết Kim Loại
Liên kết kim loại, nghe cái tên đã thấy “kim loại” rồi, đúng không nào? Vậy nó khác gì với các loại liên kết khác như liên kết cộng hóa trị hay liên kết ion? Câu trả lời nằm ở chính cách các nguyên tử kim loại tương tác với nhau. Chúng không chia sẻ electron như trong liên kết cộng hóa trị, cũng không trao đổi electron để tạo thành ion như trong liên kết ion. Thay vào đó, các nguyên tử kim loại góp chung các electron hóa trị của mình tạo thành một “biển electron” bao quanh các ion dương. Lực hút tĩnh điện giữa biển electron linh động này và các ion dương cố định chính là “chất keo” gắn kết các nguyên tử kim loại lại với nhau, hình thành nên liên kết kim loại.
Vậy, câu hỏi đặt ra là, tại sao các electron hóa trị lại có thể tự do di chuyển như vậy? Điều này là do năng lượng ion hóa của kim loại tương đối thấp, nghĩa là các electron hóa trị dễ dàng tách khỏi nguyên tử và trở thành electron tự do. Sự di chuyển tự do này của electron cũng chính là yếu tố then chốt quyết định nhiều tính chất đặc trưng của kim loại.
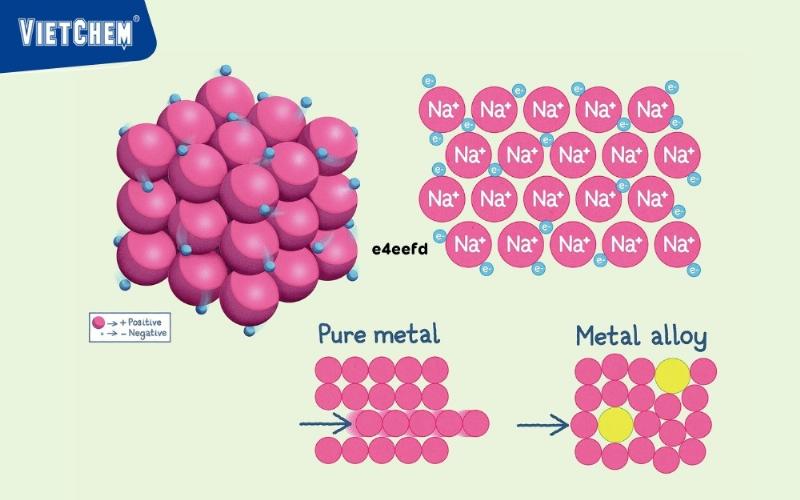
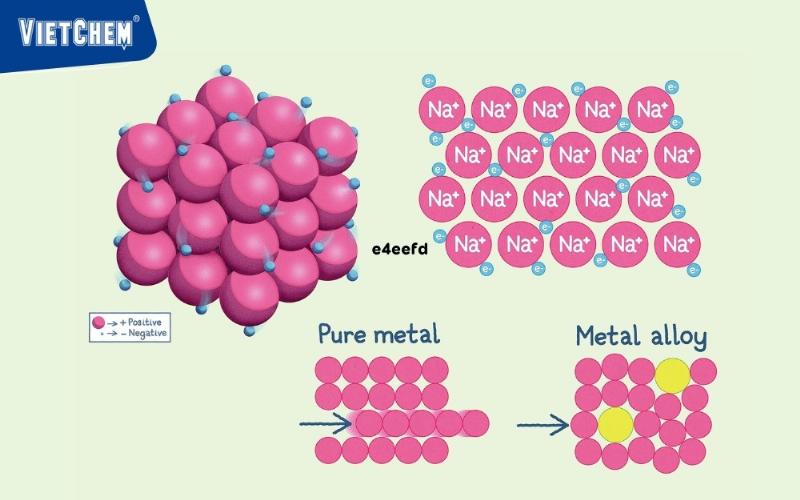 Biển Electron trong Liên Kết Kim Loại
Biển Electron trong Liên Kết Kim Loại
Tính Chất Đặc Trưng của Kim Loại: Tất Cả Nhờ Liên Kết Kim Loại
Chắc hẳn bạn đã từng nghe đến những tính chất đặc trưng của kim loại như tính dẻo, tính dẫn điện, tính dẫn nhiệt. Nhưng bạn có biết rằng chính liên kết kim loại là “thủ phạm” tạo nên những tính chất này?
Tính Dẫn Điện và Dẫn Nhiệt: Nhờ Biển Electron Linh Động
Hãy tưởng tượng biển electron như một dòng sông chảy xiết. Khi ta đặt một hiệu điện thế vào kim loại, các electron tự do này sẽ di chuyển có hướng, tạo thành dòng điện. Tương tự, khi ta đốt nóng một đầu của thanh kim loại, năng lượng nhiệt sẽ được truyền đi nhanh chóng nhờ sự di chuyển hỗn loạn của các electron tự do. Chính vì vậy, kim loại là chất dẫn điện và dẫn nhiệt tốt. Ví dụ, đồng được sử dụng rộng rãi trong dây điện chính là nhờ tính dẫn điện tuyệt vời của nó.
Tính Dẻo: Khả Năng Biến Dạng Kỳ Diệu
Bạn đã bao giờ tự hỏi tại sao ta có thể dát mỏng vàng thành lá vàng, hoặc kéo đồng thành sợi dây điện? Đó chính là nhờ tính dẻo của kim loại. Khi ta tác dụng lực vào kim loại, các lớp ion dương có thể trượt lên nhau mà không làm phá vỡ liên kết kim loại, bởi vì biển electron luôn sẵn sàng “bôi trơn” và duy trì lực hút giữa các ion. Chính nhờ tính dẻo này mà kim loại được ứng dụng rộng rãi trong nhiều lĩnh vực, từ xây dựng đến chế tạo đồ trang sức.
Liên Kết Kim Loại Trong Đời Sống: Ứng Dụng Vô Tận
Từ những vật dụng quen thuộc hàng ngày như nồi niêu xoong chảo, đến những công trình kiến trúc đồ sộ, đâu đâu ta cũng thấy sự hiện diện của kim loại. Tất cả là nhờ những tính chất đặc biệt mà liên kết kim loại mang lại.
Trong Công Nghiệp: Vật Liệu Không Thể Thiếu
Sắt, thép, nhôm, đồng… là những kim loại được sử dụng rộng rãi trong công nghiệp. Tính bền, tính dẻo, tính dẫn điện, dẫn nhiệt tốt của chúng là những yếu tố quan trọng trong việc chế tạo máy móc, thiết bị, dây điện, và nhiều ứng dụng khác. Hãy thử tưởng tượng xem, nếu không có liên kết kim loại, liệu chúng ta có thể xây dựng những tòa nhà chọc trời hay những cây cầu vững chắc như hiện nay?
Trong Y Học: Cứu Người và Nâng Cao Sức Khỏe
Kim loại cũng đóng vai trò quan trọng trong y học. Từ những dụng cụ phẫu thuật bằng thép không gỉ, đến những thiết bị y tế hiện đại, kim loại giúp các bác sĩ chẩn đoán và điều trị bệnh hiệu quả hơn. Ví dụ, titan, một kim loại có tính tương thích sinh học cao, được sử dụng để chế tạo implant nha khoa và khớp nhân tạo.
 Ứng Dụng của Liên Kết Kim Loại
Ứng Dụng của Liên Kết Kim Loại
So Sánh Liên Kết Kim Loại với Các Loại Liên Kết Khác
Để hiểu rõ hơn về liên kết kim loại, chúng ta hãy so sánh nó với hai loại liên kết phổ biến khác: liên kết cộng hóa trị và liên kết ion.
Liên Kết Kim Loại vs. Liên Kết Cộng Hóa Trị
Trong liên kết cộng hóa trị, các nguyên tử chia sẻ electron để đạt được cấu hình electron bền vững. Khác với sự chia sẻ electron cục bộ này, trong liên kết kim loại, các electron hóa trị được chia sẻ chung cho toàn bộ mạng tinh thể, tạo thành biển electron di động.
Liên Kết Kim Loại vs. Liên Kết Ion
Liên kết ion được hình thành do lực hút tĩnh điện giữa các ion trái dấu. Tuy liên kết kim loại cũng dựa trên lực hút tĩnh điện, nhưng lực hút này là giữa ion dương và biển electron, chứ không phải giữa hai ion trái dấu như trong liên kết ion.
Câu Hỏi Thường Gặp về Liên Kết Kim Loại
Tại sao kim loại dẫn điện tốt?
Liên kết kim loại cho phép các electron di chuyển tự do trong mạng tinh thể, tạo điều kiện cho dòng điện chạy qua.
Vì sao kim loại có tính dẻo?
Biển electron linh động cho phép các lớp ion dương trượt lên nhau mà không làm phá vỡ liên kết, tạo nên tính dẻo cho kim loại.
Liên kết kim loại ảnh hưởng đến độ cứng của kim loại như thế nào?
Sức mạnh của liên kết kim loại ảnh hưởng trực tiếp đến độ cứng của kim loại. Liên kết càng mạnh, kim loại càng cứng.
Tại sao một số kim loại dẫn điện tốt hơn những kim loại khác?
Số lượng electron tự do và cấu trúc mạng tinh thể ảnh hưởng đến khả năng dẫn điện của kim loại.
Làm thế nào để xác định một chất có liên kết kim loại hay không?
Các chất có liên kết kim loại thường có tính dẫn điện, dẫn nhiệt tốt, có ánh kim và tính dẻo.
Kết Luận
Liên kết kim loại, với biển electron linh động và lực hút tĩnh điện, là nền tảng cho những tính chất đặc trưng của kim loại, từ tính dẫn điện, dẫn nhiệt đến tính dẻo. Hiểu rõ về liên kết kim loại giúp chúng ta hiểu hơn về thế giới vật chất xung quanh và ứng dụng hiệu quả những vật liệu kim loại trong cuộc sống. Hãy cùng HSE tiếp tục khám phá những điều thú vị về khoa học vật liệu và chung tay bảo vệ môi trường nhé! Bạn có kinh nghiệm thú vị nào về ứng dụng của kim loại trong đời sống? Hãy chia sẻ với chúng tôi!
